W4——毒作用机制
前言
中毒是有毒物与机体交互作用,导致机体的功能或结构产生不良改变的结果。除与机体自身有关外,主要取决于毒物暴露的程度与途径。
阐明毒物作用机制,对于特定毒物的潜在危险性具有重要意义
分为四个阶段:
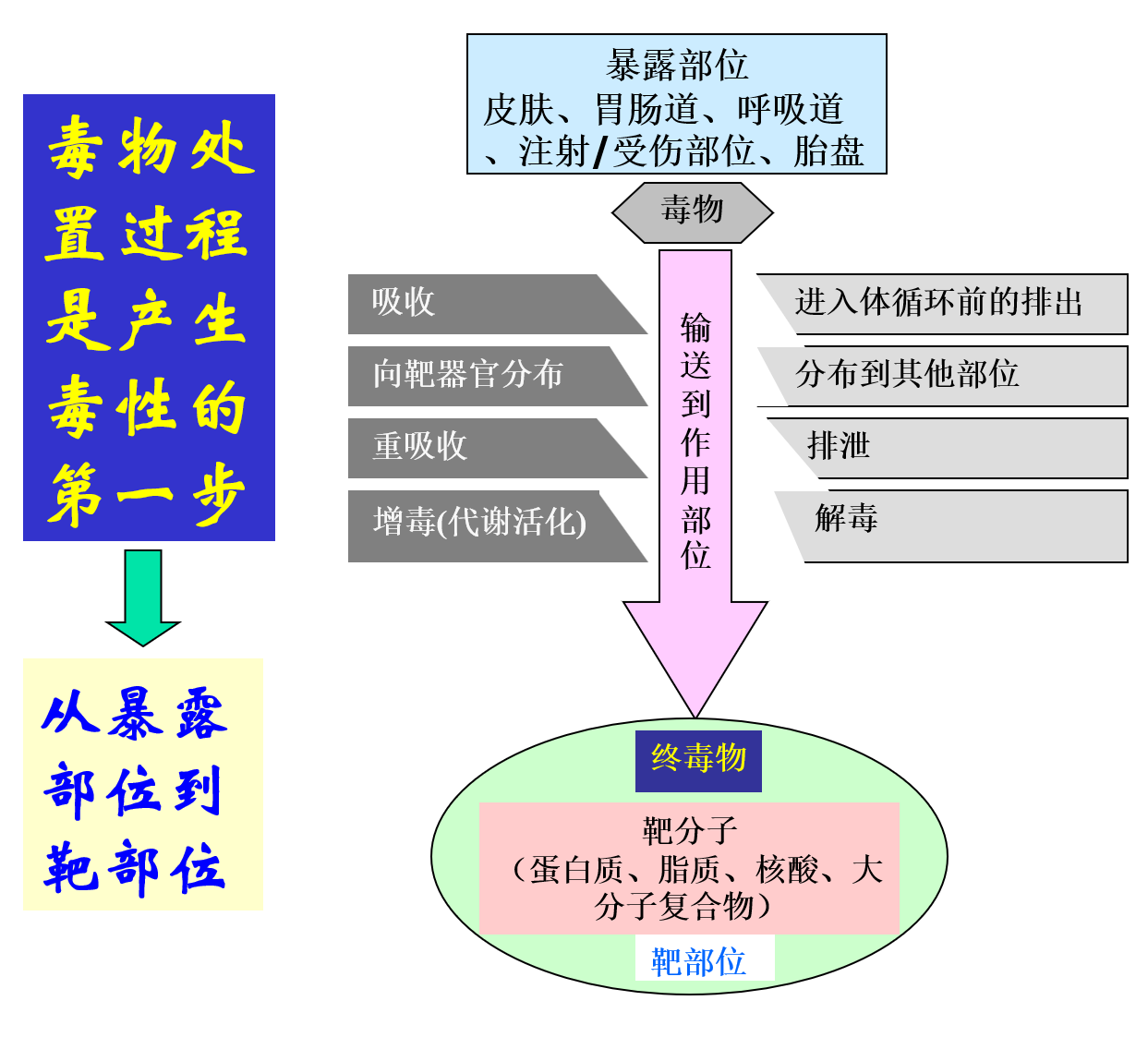
1、毒物转运:从暴露部位到靶部位
2、终毒物与靶分子的反应
3、机体各水平的功能和结构紊乱
4、修复
从整体水平、器官水平、细胞水平和分子水平不同层次解释和阐明毒作用机制
第一节 药物的ADEM过程与靶器官
基本概念
终毒物(ultimate toxicant)
直接与生物靶分子反应或引起机体生物学微环境改变、导致机体结构和功能紊乱、表现毒物毒性作用的化学物
化学毒物原型、代谢产物
转化过程生成的活性氧、活性氮或内源性分子
促进终毒物在其靶部位蓄积的因素
毒物的吸收
作用部位的分布
重吸收
增毒(代谢活化)
减少终毒物在其靶部位蓄积的因素
毒物进入体循环前的排除
从作用部位分布到其他部位
排泄与解毒
一、毒物在体内转运和转化
(一)毒物的吸收和进入体循环前的消除
毒物的吸收
毒物从接触部位进入血液循坏的过程
脂溶性
毒物进入体循环前的消除
毒物从暴露部位转运到体循环的过程中可能被消除
(二)从血液循环进入靶部位
影响毒物分布的因素:脂溶性、分子大小与形状和电离度
促进毒物分布到靶部位的机制
毛细血管内皮的多孔性;专一化的膜转运;细胞器内蓄积;
**可逆性细胞内结合
妨碍毒物分布到靶部位的机制
血浆蛋白结合;专一性屏障;贮存部位的分布;
**与细胞内结合蛋白结合;从细胞内排出
排泄
毒物及其代谢产物从血液种消除并返回外环境的过程
重吸收
转运到肾小管的毒物可穿越肾小管细胞扩散会小管外周毛细血管
二、增毒与解毒作用
终毒物的形成
终毒物可为机体所暴露的原化学物(母化合物);而另外一些毒物的毒性主要是由于其代谢物引起。毒物在体内经生物转化为终毒物的过程称为增毒(toxication)
终毒物类型
亲电子剂(electrophiles)
自由基(free radicals)
亲核物(nucleophiles)
氧化还原反应物(redox-active reductants)
亲电子剂
含有一个缺电子原子的分子,通过与亲核物中的富电子原子共享电子对而发生反应
插入一个氧原子,氧原子从其附着的原子中抽取一个电子,使其具有亲电性
共轭双键形成
通过氧的去电子作用而被极化,使得双键碳之一发生电子缺失
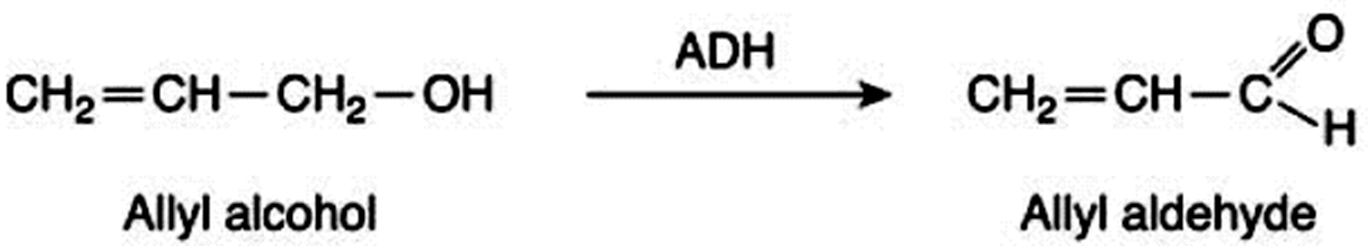
键异裂形成阳离子亲电物
金属汞氧化为Hg2+
CrO42-还原为Cr3+
AsO43-还原为AsO32+/As3+
自由基
外层轨道中含有一个或多个不成对电子的分子或分子片断
通过接受一个电子、丢失一个电子或化合物的共价键发生均裂而产生
特点:具有顺磁性,性质活泼、反应性极高,半减期极短,作用半径短
常见自由基:
超氧阴离子自由基
羟自由基
碳酸盐阴离子自由基
二氧化氮
一氧化氮
三氯甲基自由基
过氧亚硝基自由基 ONOO-
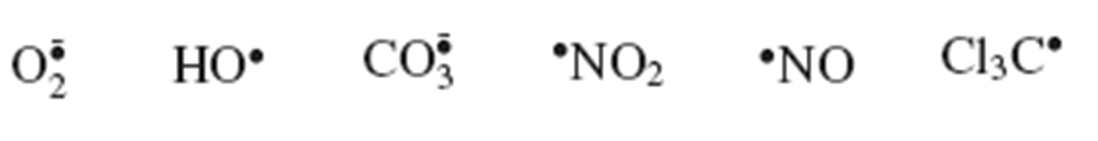
形成机理
毒物从还原酶接受一个电子后形成自由基
亲核毒物在过氧化物酶催化下丢失一个电子而形成自由基
儿茶酚类/氢醌连续两次单电子氧化,产生半醌自由基,继而形成醌
电子向分子转移引起的还原性键均裂过程形成自由基
亲核物
较少见的毒物活化作用机制
丙烯腈环氧化后和谷胱甘肽结合形成氰化物
硝普钠经巯基诱导降解后形成氰化物
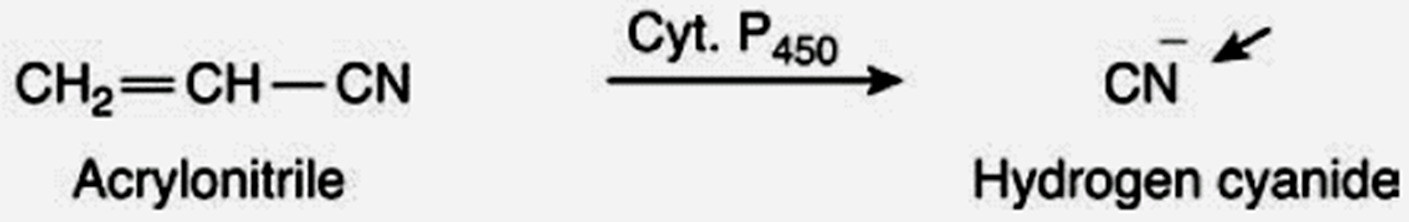
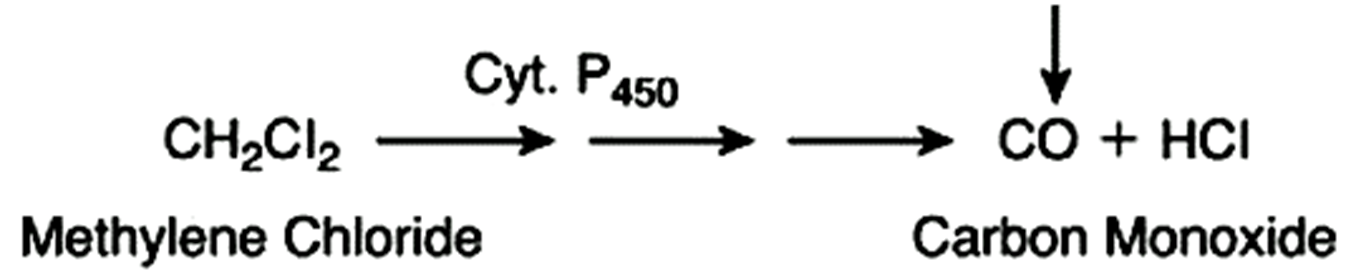
CO是二卤甲烷经过氧化脱卤的有毒代谢产物
硒化氢由亚硒酸盐与谷胱甘肽等巯基反应形成
活性氧化还原反应物
特殊的机制
亚硝酸盐:通过肠道细菌还原硝酸盐;
亚硝酸酯与谷胱甘肽反应
维生素C、还原酶(如NADPH依赖性黄素酶)
使Cr6+还原为Cr5+
解毒作用
消除终毒物,或者阻止终毒物生成的生物转化过程——解毒(detoxication)
无功能基团毒物的解毒
以两相反应解毒。细胞色素P-450酶将功能基团引入分子中,结合反应,形成失活的、高亲水的、易排泄的结合物而解毒
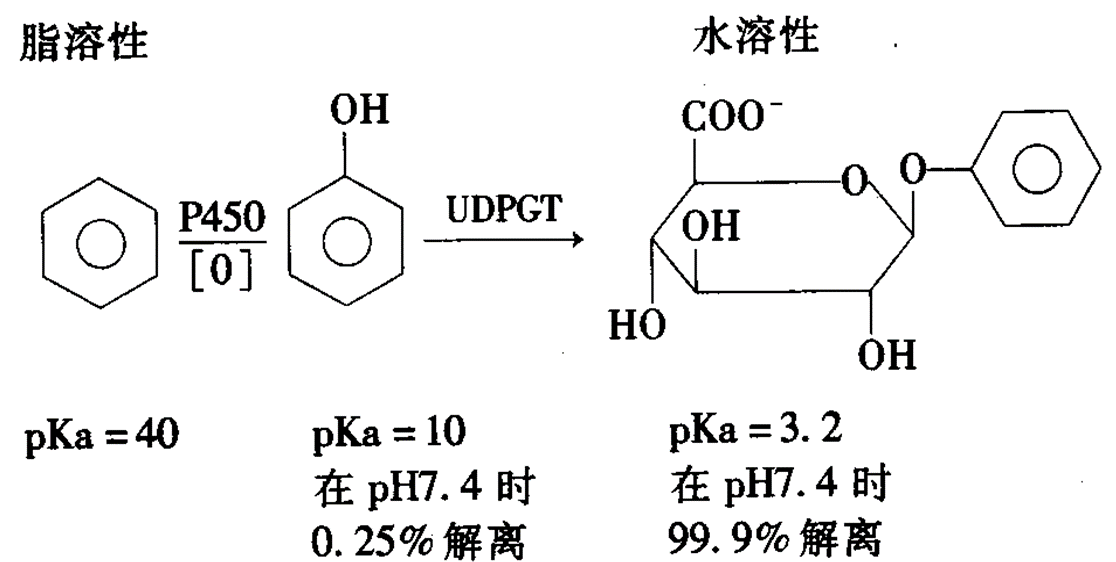
亲核物的解毒
1、通过在亲核功能基团上的结合反应解毒
2、羟基化合物:硫酸、葡萄糖醛酸结合、偶尔通过甲基化作用
3、巯基化合物:甲基化或葡萄糖醛酸化
4、胺类和肼类:乙酰基化
亲电子剂的解毒
1、与巯基亲核物谷胱甘肽结合而解毒,自发或经谷胱甘肽-S-转移酶催化
2、金属离子(如Ag+、Cd2+、Hg2+等 )易与谷胱甘肽结合而解毒
自由基的解毒
1、O2-·的排除
通过胞浆(CuZnSOD)和线粒体(MnSOD)中的超氧化物歧化酶(SOD) 来实施
SOD将O2-·转变为H2O2 ,再经谷胱甘肽过氧化物酶(GPO)或过氧化物酶体系中的过氧化氢酶(CAT)还原为水
2、OH·的排除
OH·的半衰期极短(10-9s),没有任何酶能消除OH·
**消除其前体H2O2**是惟一有效手段(过氧化氢酶、谷胱甘肽过氧化物酶可将其分解成水和氧)
谷胱甘肽消除自由基时,其自身被氧化,但可被谷胱甘肽还原酶所逆转
解毒过程失效
1、解毒能力耗竭,解毒失效,终毒物的蓄积
接触过量毒物
引起解毒酶耗竭
共底物的消耗
细胞抗氧化剂的耗竭
2、解毒酶失活
ONOO-使MnSOD失效
3、某些结合反应可被逆转
α-萘胺在肝被N-羟化并进行葡萄糖醛酸结合,以葡萄糖苷酸形式排泄到尿中。而在膀胱中,葡萄糖苷酸被水解,释放的芳基羟胺经质子化过程和脱水过程转变为具有反应性的亲电子芳基硝鎓离子
4、解毒过程产生潜在有害副产物
GSSG与蛋白巯基形成混合二硫化物;谷胱甘肽硫基自由基(GS·)与硫醇盐(GS-)反应形成谷胱甘肽二硫化物自由基阴离子(GSSG-·),使O2还原为O2-·
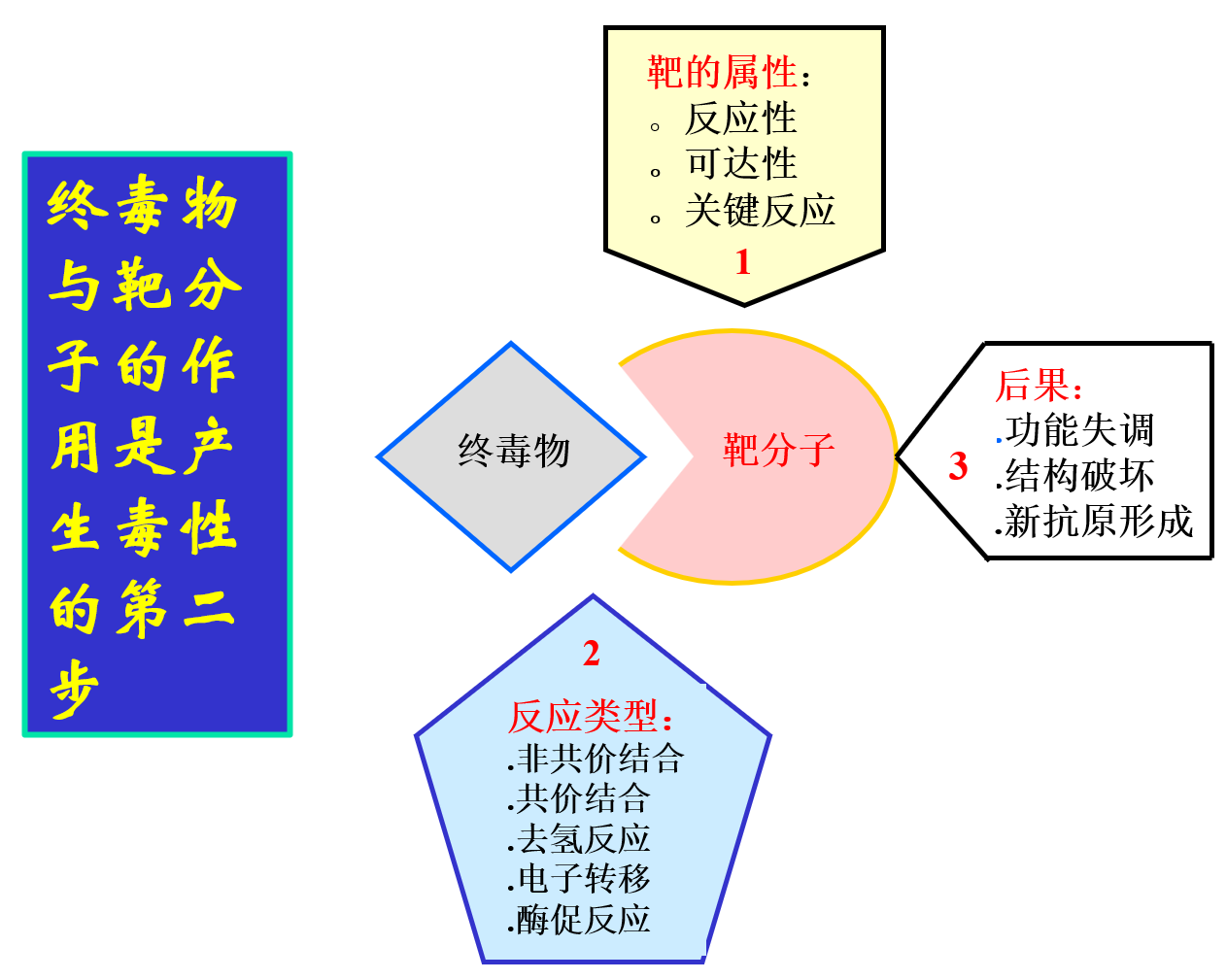
第二节 靶分子的反应
毒性是终毒物与靶分子反应所介导的一系列继发生化事件,导致靶分子本身、细胞器、细胞、组织和器官甚至整个机体的结构损伤和功能失常
实际上所有的内源化合物都是毒物潜在的靶标,然而毒理学上相关的靶标多是大分子,如核酸(特别是DNA)和蛋白质。在小分子中,膜脂质最为常见。
并非所有的化学物与靶分子结合都发生毒效应。
确定毒作用靶分子的标准
终毒物与靶标反应并对其功能产生不良影响
终毒物在靶部位达到有效的浓度
终毒物以某种机制、与所观察的毒性相关的方式改变靶分子
一、终毒物与靶分子反应类型
非共价结合
通过非极性交互作用或氢键与离子键等非共价结合方式与膜受体、细胞内受体、离子通道以及某些酶等靶分子结合
外源化学物原子的空间排列使它们与内源性分子的互补部位结合,因而表现出毒性效应
由于非共价结合的能量相对较低,所以这种结合一般是可逆的
共价结合
不可逆且持久地改变内源分子
常见于亲电子剂,与生物大分子中的亲核原子反应
其选择性取决于电荷/半径比
去氢反应

电子转移

酶促反应

二、终毒物对靶分子的有害影响
1、靶分子功能失调
(1)毒物模拟内源性配体,活化靶蛋白分子
吗啡、二氢埃托啡激活阿片受体
氯贝丁酯是一种过氧化物酶体增殖物激活剂受体的激动剂
佛波酯和铅离子激活蛋白激酶C
(2)毒物抑制靶分子的功能
阿托品、箭毒和士的宁附着于配体结合部位
或通过干扰离子通道而阻断神经递质受体
河豚毒素和蛤蚌毒素抑制神经元膜上电压激活的钠通道开放
(3)毒物与蛋白质交互作用而改变其结构,功能即发生损害
蛋白质的巯基极易与毒物发生共价结合或发生氧化修饰
(4)毒物干扰DNA的模板功能
化学物与DNA共价结合引起复制期间核苷酸错配。黄曲霉毒素诱发的ras原癌基因及p53肿瘤抑制基因突变的出现
2、靶分子的结构破坏
(1)毒物通过与内源性分子形成加合物、发生交联和断裂而改变内源分子的一级结构
ü2,5-己二酮、二硫化碳、丙烯醛、4-羟壬醛和氮芥烷化剂能交联细胞骨架蛋白、DNA,或使DNA与蛋白质交联
(2)靶分子在毒物作用下发生自发性降解
自由基(CL3COO·和OH·)引起脂肪酸脱氢而启动脂质的过氧化降解,所形成的脂质自由基(L·)紧接着通过氧固化作用转变为脂质过氧自由基(LOO·),……断裂形成烃和活性醛
(3)毒物可引起DNA断裂
DNA碱基受OH·自由基攻击后形成咪唑环开放的嘌呤或环收缩的嘧啶,导致复制障碍
电离辐射产生的多种羟自由基攻击较短的DNA引起双链断裂,导致细胞死亡
3、新抗原形成
外源化学物或其代谢物与生物大分子共价结合,在少数个体可作为新抗原激发免疫应答
本身具有与蛋白质结合的能力:青霉素 硝基氯苯
自氧化为醌类或转化为代谢产物后才能与蛋白质结合
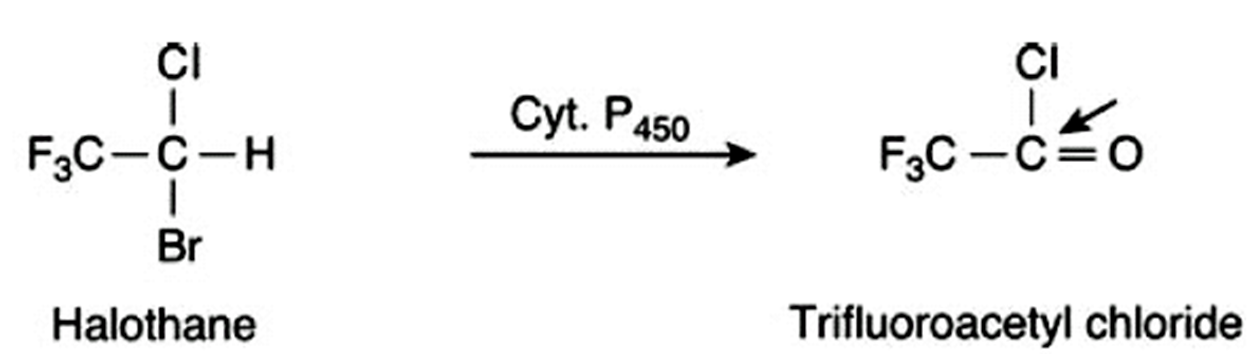
氟烷转化为三氟乙酰氯,作为半抗原与肝微粒体和细胞表面蛋白质结合,诱导抗体产生,肝炎样综合征
第三节 细胞调节功能障碍(自学)
毒物与靶分子反应并导致细胞功能损害,是毒性发展过程的第三个阶段
机体的每个细胞都执行着特定的程序
决定细胞的命运(增殖、分化或凋亡)
控制细胞的瞬息活动,决定细胞分泌活性物质的种类和数量;是否收缩或舒张;转运和代谢营养物质的速率等