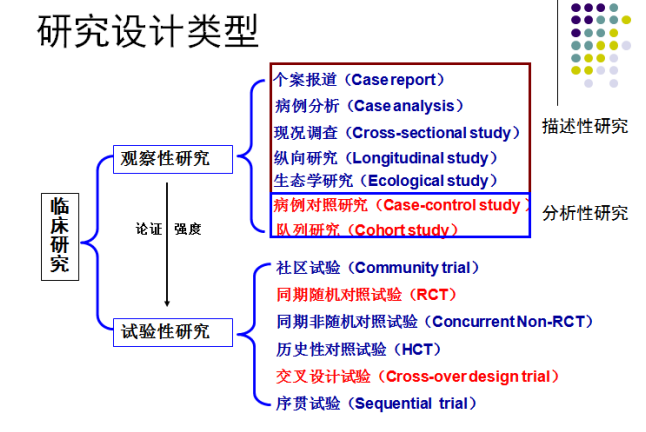
W5-实验性研究
概述
基本概念
观察(observation)是在不干预的自然情况下认识自然现象的本来面目。
实验(experiment)是采用一些人为的方法改变自然现象,从而使一些本来在自然情况下并不显露的现象显示出来。
(从现在开始)(有干预)
(条件根据人决定,精确严谨性不足,称为trial试验)
定义
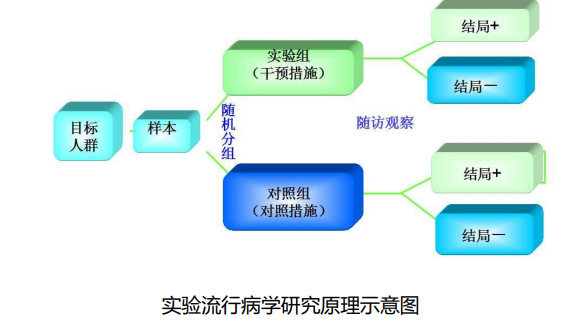
实验流行病学( experimental epidemiology 研究又称干预试验 (interventional trial),是指研究者根据研究目的,按照预先确定的研究方案将研究对象随机分配到试验组和对照组,对试验组人为地施加或减少某种因素,然后追踪观察该因素的作用结果,比较和分析两组或多组人群的结局,从而判断干预措施的效果。
基本特点
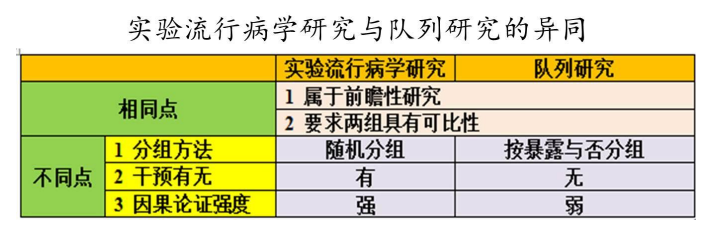
(1)属于前瞻性研究
(2)随机分组
(3)具有均衡可比的对照组
(4)有人为施加的干预措施
主要类型
(一)临床试验(clinical trial)
(二)现场试验(field trial)
(三)社区干预试验(community intervention trial)
临床试验
临床试验(clinical trial) 是以已确诊患有某病的病人作为研究对象,以临床治疗措施(药物或治疗方案)为研究内容,通过观察和比较试验组和对照组的临床疗效和安全性,从而对临床各种治疗措施的效果进行科学评价。在临床试验时,首先从具有临床症状的大量病人中选出合适的研究对象,然后将研究对象分为两组或多组:一组为试验组,给予某种干预措施(新药或新疗法),另一组为对照组,给予安慰剂或传统疗法。
基本特点
- 以病人为研究对象
- 研究多在医院进行
- 多为治疗性试验
- 研究对象尽可能在基线特征方面一致
- 随机分配治疗措施
- 尽可能使用盲法
- 如果对于所研究的疾病没有接受的疗法,可以考虑应用安慰剂
基本原则
(一)随机化原则
(二)对照原则
(三)盲法原则
(四)重复原则
分期
Ⅰ期临床试验:通常是指在10~30例志愿者身上进行初步的临床药理学及人体安全性评价试验;
Ⅱ期临床试验:通常是指以100~300例病人作为研究对象,对治疗作用进行初步评价;
Ⅲ期临床试验:治疗作用确证阶段;多中心(≥3个);
Ⅳ期临床试验:新药上市后的应用研究阶段。属于上市后临床试验(postmarketing clinical trial)
现场试验
现场试验(field trial)也叫人群预防试验(prevention trial),是以尚未患病的人作为研究对象。与临床试验一样,现场试验中接受处理或某种预防措施的基本单位是个体,而不是亚人群
基本特点
- 研究对象为非病人
- 研究多在医院社区、学校、工厂等
- 多为预防性试验
- 通常需要较多的研究对象
- 需要以个体为单位随机分配措施
- 对分配措施的不依从,应当测量其程度和原因
- 尽可能使用盲法
社区试验
社区试验(community trial)也叫社区干预项目(community intervention program,CIP),是以人群作为整体进行试验观察,常用于对某种预防措施或方法进行考核或评价。整体可以是一个社区,或某个人群的亚人群,比如说学校的班级、某工厂的车间等
基本特点
- 研究场所为社区等
- 以社区人群或某类人群组/亚组为单位分配干预措施
- 常用于某种预防措施或方法的考核或评价
- 整群随机分配
- 如果研究只包含两个社区,干预社区与对照社区间基线特征有类似的分布

研究设计与实施
必须撰写研究方案 study protocol
必须撰写项目工作手册
必须经伦理委员会同意
必须要在临床试验注册网上注册,获得注册号
考虑投稿发表Protocol,有风险
人力、物力、财力
Clinical trial 看起来不错,做起来困难!
(一)确定研究的问题和目的
Protocol 里的研究背景及意义(起底文献)
确定自己计划干什么 what?
1、基础研究的提示
2、 动物实验结果在人体的进一步验证
3、 临床医生的实际观察和总结
4、 人群流行病学的观察和研究
无论如何,其创新性及实用性是必不可少的
在此基础上,构建临床研究问题和确定研究目的!

(二)确定试验现场
1、人口相对稳定,流动性小
2、有较高而稳定的事件发生率
3、评价疫苗效果时,近期应无该疾病流行
4、较好的医疗卫生水平
5、领导重视、群众容易接受
(三)研究对象的确定
选择研究对象的主要原则:
1. 选择对干预措施有效的人群
2. 选择预期发病率较高的人群
3. 选择干预对其无害的人群
4. 选择能将试验坚持到底的人群
5. 选择依从性好的人群
Criteria:诊断标准+入选标准+排除标准
Where:社区 or 三级?门诊 or 住院?
When:起止时间 e.g. 2018.09-2019.09
How :随机入选?连续入选?
Recruitment: 招募方式
排除标准 Exclusion Criteria
同质性:临床特征基本相同,容易出差异。
弱势群体:孕妇、青少年儿童等
竞争风险:肿瘤;肝肾功能不全
不良事件风险:胃出血患者不能作为溶栓的研究对象.
不能合作者、难以随访者:head nurse,coordinator
不同意参加研究者:不签署知情同意书
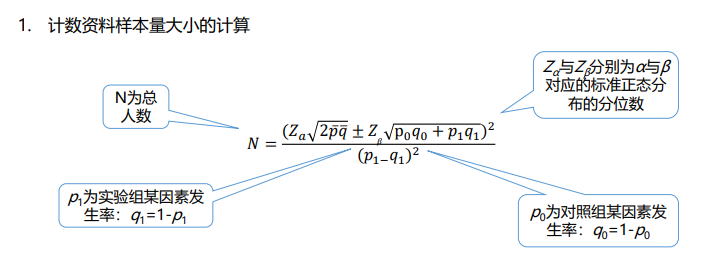
(四)确定样本量
决定样本量大小的因素包括:
1. 试验组和对照组差异的大小;
2. 在计数资料中,结局事件在人群中发生的频率决定样本量的大小;
3. 在计量资料中,个体间的差异(即方差或标准差)决定样本量的大小;
4. 检验的显著性水平α(Ⅰ类错误的概率)和检验效能1-β(β为Ⅱ类错误的概率);
5. 单侧检验或双侧检验影响样本量的大小。
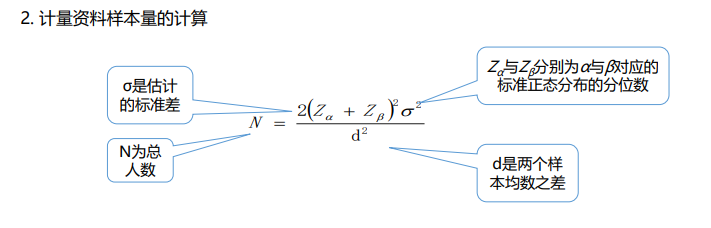
(五)试验药物或干预措施的选择
要有科学的证据。要有临床前期的观察,证明其有效性和安全性。
具有一定的创新性。
符合医学伦理,是患者,遵循赫尔辛基宣言(The declaration of Helsinki)
(六)结局的确定和测量
结局:特指干预可能影响或改变的事件、指标或变量,一项干预措施的实施可能影响的结局是多种的,有些是与疾病和健康有直接相关的结局;有些是干预产生的间接结果
主要结局:1-2个
次要结局:N 个
临床试验两方面结局:有效性+安全性
事件获取的标准流程……
终点事件确认委员会:5个专家左右,包含不同专业
样本量的计算以主要结局为主
(七)随机化
随机化(randomization):将研究对象随机分配到实验组和对照组,使每个研究对象都有同等的机会被分配到各组去,以平衡实验组和对照组各种已知和未知的混杂因素,提高组间可比性
- 简单随机化(simple randomization)
- 区组随机化(block randomization)
- 分层随机化(stratified randomization)
临床试验很难做到随机抽样!都是连续入选
随机不等于“随意”或“随便”
随机化隐匿: 为了防止招募病人的研究者和病人在分组前知道随机分组的方案,一种防止随机分组方案提前解密的方法称之为随机分组治疗方案的隐匿,简称为分组隐匿; 采用分组隐匿的随机分组成为隐匿随机分组。
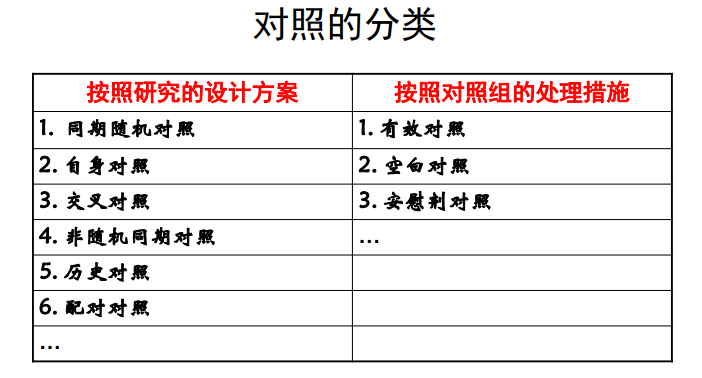
(八)对照
设立对照的意义
1、不能预知的结局
由于个体的生物学变异和社会、心理因素的影响,导致临床上患相同疾病的个体,其临床特征(临床表现、病情轻重、 预后等)存在较大差异
2、霍桑效应
指人们因为研究中特别感兴趣和受关注的对象而产生的一种正向心理---生理效应,这种效应与他们接受的干预措施的作用性无关。
3、安慰剂效应
某些研究对象,即使仅使用了安慰剂,也可能表现出病情好转等不该有的效果,其实质是某些研究对象由于依赖医药而产生的一种正向心理效应。
4、向均数回归现象
指一些极端的临床症状和体征向均数的接近的倾向。
举例:如血压水平处于高限5%的人,即使不给任何处理,经过一段时间,血压值也会下降(向均数靠近)。
5、潜在未知因素的影响
由于知识的局限性,很可能存在一些影响干预效应的因素, 但目前尚未被人们所认识。
(九)盲法的应用
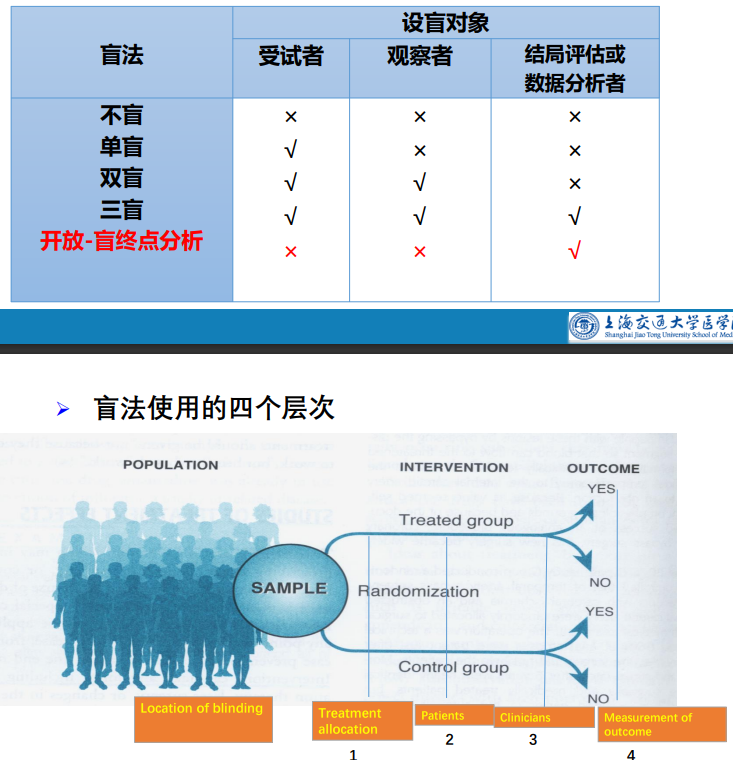
详见书P119
(十)确定试验观察期限
随访时间的长短需要兼顾科学性和可行性的原则:
1、 观察期过长,会造成不必要的浪费;
2、过短则可能会使药物或措施致假阴性效果。
3、一般情况下,有规定的终止时间;但是也有例外(结果已 出现、严重不良反应等)。
(十一)资料收集
收集哪些资料?
如何收集资料?
什么时间收集资料?
研究测量标准化?

资料整理与分析
资料的整理
材料:病历、观察表、临床化验、各种功能检查。
核查、录入、保存。
排除exclusion:在随机分组研究对象因各种原因没有被纳入。内部真实性不受影响,外推性受限。
退出withdraw
不合格研究对象:资料整理时,一般建议剔除,包括不符合纳入标准者或一次也没有接受干预措施或没有任何数据者。
不依从研究对象:随机分组后,不遵守试验所规定的要求。干预组和对照组都可能出现不依从,一般不能剔除。
失访:研究对象因迁移或与本病无关的其他疾病死亡等而造成失访。尽量减少失访,建议失访率<10%。
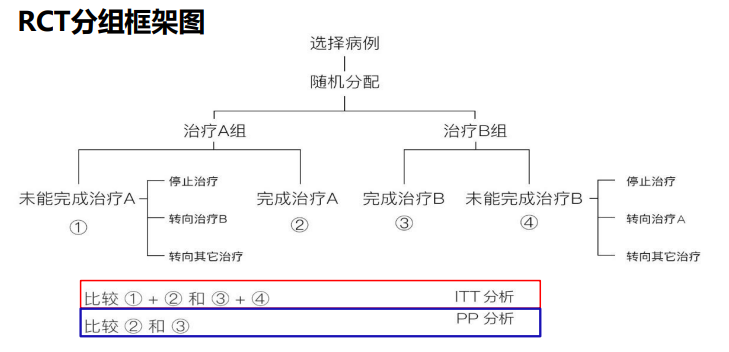
意向治疗分析
将试验所有纳入随机分配的病人,不管是否最后是否接受到分配的治疗,在最后资料分析中都应按随机分配方案统计。该方法可以保证结论更真实、可靠。
这种分析方法维持了原来两组研究对象的可比性,并为统计学检验提供了可靠的基础。结果一般是保守的,往往会低估干预措施的真实效果,但是最科学
符合研究方案(Per-protocol, PP)分析
只比较②组和③组。它只对依从了干预措施的研究对象进行分 析,但由于剔除了依从性差或不依从者,可能会高估药物上市后 的真实疗效。
统计分析数据集
- FAS 集 全分析集(Full analysis set,FAS),基于意向性原则,全部随机化的受试者都应该纳入分析,常称之为ITT人群。FAS集是从所有随机化的受试者为基础,以最少的和合理的方法剔除受试者后得出的。剔除理由:不符合入选标准的受试者;入组后没有任何的随访记录者。
- PPS集 符合方案集(Per-protocol set,PP),基于符合方案集原则,全部随机化的受试者中,完全按照方案设计进行研究的那一部分才能纳入分析。 一般没有重要违背方案的都认为是符合方案。
- SAS集 安全性分析集(Safety analysis set,SAS),即至少使用过一次研究药物的受试者,都必须观察安全性指标,无论是否遵从原试验方案。


常见偏倚及其控制
(一)常见偏倚
- 失访 指研究对象因迁移或其他疾病死亡等而造成失访,从而破坏了原有样本的代表性。
- 干扰 指试验组额外接受了与实验效应一致的其他处理措施,从而造成人为夸大疗效的假象。
- 沾染 指对照组患者额外地接受了试验组药物,造成人为夸大对照组疗效,从而低估效应的现象。
(二)控制偏倚
- 排除(exclusion) 在随机分配研究对象之前,应进一步筛查研究对象,凡是治疗或干预措施的禁忌证者、无法追踪者、可能失访者、拒绝参加者以及不符合标准的研究对象,均应予以排除。
- 提高试验对象的依从性(compliance) 临床依从性是指患者在临床试验中执行医嘱的程度。
- 降低试验对象的失访率 在临床试验研究中尽量减少失访,一般要求失访率不超过10%。
小结
实验流行病学研究是重要的流行病学研究方法之一。 具有随机分组、设立对照、人为施以干预措施、前瞻性四个主要特点。实验流行病学研究的主要类型包括临床试验、现场试验和社区干预试验。临床试验常用于评价治疗措施的效果。现场试验主要用于评价疫苗或药物在人群中预防疾病的效果,而社区干预试验则用于评估人群干预措施的效果。实验流行病学在设计中应用了随机分组,有效控制了混杂偏倚对研究结果的影响,并且可以获得一种干预与多种结局之间的关系,但实施难度大